07
Thủ tục đăng ký lưu hành trang thiết bị y tế sản xuất trong nước
- 6553 lượt xem
- 0 bình luận
- 10:22 17/07/2017
Trang thiết bị y tế sản xuất trong nước phải được Bộ Y tế cấp số đăng ký lưu hành mới được lưu thông trên thị trường. Chính vì thế, để rút ngắn thời gian cũng như chi phí khi thực hiện, các doanh nghiệp cần tìm hiểu kỹ về thủ tục đăng ký lưu hành trang thiết bị y tế sản xuất trong nước. Hiểu được điều đó, Everestlaw sẽ cung cấp những thông tin cần thiết nhất về thủ tục cho các doanh nghiệp trong bài viết dưới đây.
Xem thêm:
Thủ tục đăng ký lưu hành trang thiết bị y tế sản xuất trong nước
1. Thủ tục đăng ký lưu hành trang thiết bị y tế sản xuất trong nước
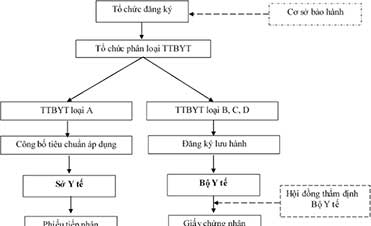
Thủ tục đăng ký lưu hành trang thiết bị y tế được hướng dẫn tại Thông tư 07/2002/TT-BYT ngày 30/05/2002 của Bộ Y tế về hướng dẫn, đăng ký lưu hành sản phẩm trang thiết bị y tế. Cụ thể như sau:
- Bước 1: Cơ sở đăng ký lưu hành trang thiết bị y tế nộp hồ sơ tới Vụ Trang thiết bị và công trình y tế thuộc Bộ Y tế.
- Bước 2: Bộ Y tế sẽ xem xét và cấp số đăng ký lưu hành sản phẩm trang thiết bị y tế trong thời hạn 15 ngày làm việc kể từ ngày nhận đủ hồ sơ theo quy định, nếu không cấp sẽ trả lời bằng văn bản nêu rõ lý do.
Lưu ý: Số đăng ký lưu hành có giá trị trong 3 năm kể từ ngày cấp. Trước khi hết hạn 30 ngày, nếu vẫn tiếp tục kinh doanh, sản xuất các sản phẩm đã có số đăng ký, đơn vị phải làm thủ tục gia hạn. Trong thời gian được phép lưu hành nếu nhà sản xuất có thay đổi về mẫu mã, tính năng kỹ thuật của sản phẩm, phải có văn bản báo cáo Bộ Y tế.
2. Hồ sơ đăng ký lưu hành trang thiết bị y tế sản xuất trong nước
Hồ sơ đăng ký lưu hành trang thiết bị y tế sản xuất tại Việt Nam gồm những giấy tờ sau:
- Đơn đăng ký lưu hành sản phẩm trang thiết bị y tế.
- Giấy chứng nhận đăng ký kinh doanh, trong đó đã ghi chức năng sản xuất trang thiết bị y tế (bản sao có công chứng).
- Bản Công bố tiêu chuẩn chất lượng hàng hóa hoặc bản Công bố hàng hóa phù hợp tiêu chuẩn.
- Kết quả đánh giá thử nghiệm ở ít nhất 3 cơ sở y tế của Việt Nam (tùy theo từng loại sản phẩm, Bộ Y tế chỉ định cơ sở y tế để thử nghiệm).
- Kết quả kiểm nghiệm các tính chất hóa, lý và kiểm định độ an toàn của cơ quan chức năng (đối với những loại sản phẩm có yêu cầu kiểm nghiệm, kiểm định).
- Tài liệu kỹ thuật, hướng dẫn sử dụng.
- Nhãn sản phẩm: Theo đúng quy định hướng dẫn tại Nghị định 89/2006/NĐ-CP ngày 30/08/2006 của Chính phủ về nhãn hàng hoá và Thông tư 09/2007/TT-BKHCN ngày 06/04/2007 của Bộ Khoa học công nghệ.
3. Dịch vụ đăng ký lưu hành trang thiết bị y tế sản xuất trong nước
Dịch vụ xin giấy phép lưu hành trang thiết bị y tế sản xuất trong nước của Everestlaw với nhiều năm kinh nghiệm và đã hỗ trợ cho rất nhiều đơn vị kinh doanh thiết bị y tế trên cả nước. Cụ thể như sau:
- Tư vấn về quy định, yêu cầu, các điều kiện về hồ sơ, trình tự xin cấp giấy phép lưu hành trang thiết bị y tế;
- Thẩm định và đánh giá toàn bộ tài liệu đã có và thông tin sản phẩm của khách hàng;
- Tư vấn điều chỉnh, bổ sung trong trường hợp thong tin, tài liệu đã có chưa đáp ứng được quy định về đăng ký lưu hành trang thiết bị y tế của Bộ y tế;
- Soạn thảo các văn bản cần thiết và tập hợp đầy đủ hồ sơ hợp lệ;
- Đại diện doanh nghiệp nộp hồ sơ tại cơ quan nhà nước và thúc đầy hoàn thành công việc sớm hơn hoặc theo thời hạn đã cam kết với khách hàng;
- Bàn giao kết quả là Giấy phép lưu hành trang thiết bị y tế cho khách hàng;
Đừng ngần ngại hãy liên hệ ngay tới 037-2205-204 để được tư vấn cụ thể và chi tiết nhất về thủ tục đăng ký lưu hành trang thiết bị y tế sản xuất tại Việt Nam.