Căn cứ pháp lý
Nghị định 36/2016/NĐ-CP về quản lý trang thiết bị y tế
Nghị định 169/2018/NĐ-CP sửa đổi Nghị định 36/2016/NĐ-CP về quản lý trang thiết bị y tế
Ngày có hiệu lực
31/12/2018
Điều kiện đối với cơ sở sản xuất trang thiết bị y tế.
Điều 12. Điều kiện về nhân sự của cơ sở sản xuất trang thiết bị y tế
1. Điều kiện của người phụ trách chuyên môn:
a) Có trình độ từ cao đẳng kỹ thuật trang thiết bị y tế trở lên hoặc trình độ từ đại học chuyên ngành kỹ thuật hoặc chuyên ngành y, dược trở lên. Đối với cơ sở sản xuất trang thiết bị y tế có chứa chất ma túy và tiền chất, người phụ trách chuyên môn phải có trình độ đại học chuyên ngành trang thiết bị y tế, y, dược, hóa học hoặc sinh học;
b) Có thời gian công tác trực tiếp về kỹ thuật trang thiết bị y tế tại các cơ sở trang thiết bị y tế từ 24 tháng trở lên;
c) Làm việc toàn thời gian tại cơ sở sản xuất. Việc phân công, bổ nhiệm người phụ trách chuyên môn của cơ sở sản xuất phải được thể hiện bằng văn bản.
2. Có đội ngũ nhân viên đáp ứng được yêu cầu sản xuất đối với loại trang thiết bị y tế mà cơ sở sản xuất.
Điều 13. Điều kiện về quản lý chất lượng của cơ sở sản xuất trang thiết bị y tế.
1. Đạt tiêu chuẩn hệ thống quản lý chất lượng theo quy định tại khoản 1 Điều 68 Nghị định này.
2. Đối với cơ sở sản xuất trang thiết bị y tế có chứa chất ma túy và tiền chất, ngoài việc đáp ứng các điều kiện quy định tại khoản 1 Điều này, phải có thêm hệ thống theo dõi quản lý quá trình xuất, nhập, tồn kho, sử dụng nguyên liệu là chất ma túy và tiền chất, quá trình xuất, nhập, tồn kho trang thiết bị y tế có chứa chất ma túy và tiền chất và kho bảo quản đáp ứng quy định tại Điều 7 Nghị định số 80/2001/NĐ-CP ngày 05 tháng 11 năm 2001 của Chính phủ hướng dẫn kiểm soát các hoạt động hợp pháp liên quan đến ma túy ở trong nước (sau đây gọi tắt là Nghị định 80/2001/NĐ-CP).
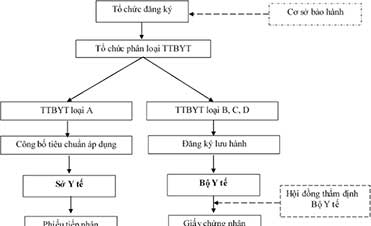
Mục 1. ĐIỀU KIỆN LƯU HÀNH, SỐ LƯU HÀNH VÀ ĐIỀU KIỆN CỦA TỔ CHỨC ĐỨNG TÊN CÔNG BỐ TIÊU CHUẨN ÁP DỤNG HOẶC ĐĂNG KÝ LƯU HÀNH
Điều 17. Điều kiện lưu hành đối với trang thiết bị y tế
1. Trang thiết bị y tế khi lưu hành trên thị trường phải đáp ứng các điều kiện sau:
a) Đã có số lưu hành hoặc đã được cấp phép nhập khẩu theo quy định tại Nghị định này, trừ khí y tế;
b) Có nhãn hoặc có kèm theo nhãn phụ với đầy đủ các thông tin theo quy định tại Điều 54 Nghị định này;
c) Có tài liệu kỹ thuật để phục vụ việc sửa chữa, bảo dưỡng trang thiết bị y tế, trừ trường hợp trang thiết bị y tế sử dụng một lần theo quy định của chủ sở hữu trang thiết bị y tế;
d) Có thông tin về hướng dẫn sử dụng của trang thiết bị y tế bằng tiếng Việt;
đ) Có thông tin về cơ sở bảo hành, điều kiện và thời gian bảo hành, trừ trường hợp trang thiết bị y tế sử dụng một lần theo quy định của chủ sở hữu trang thiết bị y tế hoặc có tài liệu chứng minh không có chế độ bảo hành;
2. Trường hợp thông tin theo quy định tại các điểm c, d và đ khoản 1 Điều này không kèm theo trang thiết bị y tế thì phải cung cấp dưới hình thức thông tin điện tử và phải thể hiện rõ hướng dẫn tra cứu thông tin trên nhãn trang thiết bị y tế.
Điều 18. Điều kiện để công bố tiêu chuẩn áp dụng hoặc cấp giấy chứng nhận đăng ký lưu hành đối với trang thiết bị y tế
1. Điều kiện để công bố tiêu chuẩn áp dụng hoặc cấp giấy chứng nhận đăng ký lưu hành đối với trang thiết bị y tế:
a) Được sản xuất tại cơ sở sản xuất đã công bố đủ điều kiện sản xuất đối với trang thiết bị y tế sản xuất trong nước;
b) Được sản xuất tại cơ sở sản xuất đã được cấp Giấy chứng nhận đạt tiêu chuẩn quản lý chất lượng và được lưu hành tại bất kỳ quốc gia nào trên thế giới đối với trang thiết bị y tế nhập khẩu;
c) Phù hợp với quy chuẩn kỹ thuật quốc gia hoặc tiêu chuẩn mà nhà sản xuất công bố áp dụng.
2. Không cho phép thực hiện lại thủ tục công bố tiêu chuẩn áp dụng hoặc đăng ký lưu hành đối với trang thiết bị y tế thuộc một trong các trường hợp sau:
a) Trang thiết bị y tế thuộc trường hợp theo quy định tại khoản 1 Điều 34 Nghị định này;
b) Trang thiết bị y tế bị thu hồi thuộc trường hợp theo quy định tại các khoản 1 và 3 Điều 35 Nghị định này.
3. Không tiếp nhận hồ sơ công bố tiêu chuẩn áp dụng hoặc đăng ký lưu hành trong thời hạn 12 tháng, kể từ ngày có quyết định thu hồi số đăng ký lưu hành đối với trang thiết bị y tế thuộc một trong các trường hợp theo quy định tại các khoản 2 và 8 Điều 35 Nghị định này.
Điều 19. Trang thiết bị y tế được miễn công bố tiêu chuẩn áp dụng và miễn đăng ký lưu hành
1. Trang thiết bị y tế chỉ phục vụ cho mục đích nghiên cứu, thử nghiệm, hướng dẫn sử dụng, sửa chữa trang thiết bị y tế.
2. Trang thiết bị y tế nhập khẩu vào Việt Nam với mục đích viện trợ hoặc để phục vụ hoạt động hội chợ, triển lãm, trưng bày, giới thiệu sản phẩm hoặc để sử dụng cho mục đích là quà biếu, cho, tặng.
3. Trang thiết bị y tế sản xuất tại Việt Nam chỉ với mục đích xuất khẩu hoặc tham gia trưng bày, hội chợ, triển lãm ở nước ngoài.
Điều 21. Điều kiện của tổ chức được đứng tên công bố tiêu chuẩn áp dụng hoặc đăng ký lưu hành trang thiết bị y tế
1. Tổ chức được đứng tên công bố tiêu chuẩn áp dụng hoặc đăng ký lưu hành trang thiết bị y tế bao gồm:
a) Doanh nghiệp, hợp tác xã, hộ kinh doanh của Việt Nam là chủ sở hữu trang thiết bị y tế;
b) Doanh nghiệp, hợp tác xã, hộ kinh doanh của Việt Nam có chức năng kinh doanh trang thiết bị y tế được chủ sở hữu trang thiết bị y tế ủy quyền đăng ký;
c) Văn phòng đại diện thường trú tại Việt Nam của thương nhân nước ngoài mà thương nhân đó là chủ sở hữu trang thiết bị y tế hoặc được ủy quyền của chủ sở hữu trang thiết bị y tế.
2. Tổ chức đứng tên công bố tiêu chuẩn áp dụng hoặc đăng ký lưu hành trang thiết bị y tế phải có cơ sở bảo hành tại Việt Nam hoặc phải có hợp đồng với tổ chức đủ năng lực bảo hành trang thiết bị y tế mà mình đứng tên đăng ký, trừ trường hợp các trang thiết bị y tế sử dụng một lần theo quy định của chủ sở hữu trang thiết bị y tế.
Trường hợp tổ chức đứng tên công bố tiêu chuẩn áp dụng hoặc đăng ký lưu hành trang thiết bị y tế thuộc quy định tại điểm c khoản 1 Điều này thì chủ sở hữu trang thiết bị y tế phải có hợp đồng với cơ sở đủ năng lực bảo hành trang thiết bị y tế mà mình đứng tên công bố hoặc đăng ký, trừ trường hợp các trang thiết bị y tế sử dụng một lần theo quy định của chủ sở hữu trang thiết bị y tế.
Cơ sở bảo hành phải được chủ sở hữu trang thiết bị y tế chứng nhận đủ năng lực bảo hành sản phẩm mà tổ chức đó đứng tên đề nghị cấp số lưu hành.
Điều 37. Điều kiện của cơ sở mua bán trang thiết bị y tế thuộc loại B, C, D
1. Có ít nhất 01 nhân viên kỹ thuật có trình độ cao đẳng chuyên ngành kỹ thuật hoặc chuyên ngành y, dược hoặc cao đẳng kỹ thuật trang thiết bị y tế trở lên hoặc có trình độ cao đẳng trở lên mà chuyên ngành được đào tạo phù hợp với loại trang thiết bị y tế mà cơ sở mua bán;
2. Có kho bảo quản và phương tiện vận chuyển đáp ứng các điều kiện tối thiểu sau đây:
a) Kho bảo quản:
- Có diện tích phù hợp với chủng loại và số lượng trang thiết bị y tế được bảo quản;
- Bảo đảm thoáng, khô ráo, sạch sẽ, không gần các nguồn gây ô nhiễm;
- Đáp ứng yêu cầu bảo quản khác của trang thiết bị y tế theo hướng dẫn sử dụng.
b) Phương tiện vận chuyển trang thiết bị y tế từ cơ sở mua bán đến nơi giao hàng phù hợp với loại trang thiết bị y tế mà cơ sở mua bán;
Trường hợp không có kho hoặc phương tiện bảo quản trang thiết bị y tế phải có hợp đồng với cơ sở đủ năng lực để bảo quản và vận chuyển trang thiết bị y tế.
3. Đối với cơ sở mua bán trang thiết bị y tế có chứa chất ma túy và tiền chất:
a) Người phụ trách chuyên môn phải có trình độ đại học chuyên ngành trang thiết bị y tế, y, dược, hóa dược hoặc sinh học;
b) Có kho bảo quản đáp ứng quy định tại Điều 7 Nghị định 80/2001/NĐ-CP;
c) Có hệ thống theo dõi quản lý quá trình xuất, nhập, tồn kho trang thiết bị y tế có chứa chất ma túy và tiền chất.
Điều 41. Xuất khẩu, nhập khẩu trang thiết bị y tế
1. Khuyến khích các doanh nghiệp trong nước sản xuất để xuất khẩu.
2. Tổ chức, cá nhân thực hiện nhập khẩu trang thiết bị y tế đã có số lưu hành phải đáp ứng các điều kiện sau:
a) Là chủ sở hữu số lưu hành hoặc có giấy ủy quyền của chủ sở hữu số lưu hành. Chủ sở hữu số lưu hành khi ủy quyền cho cơ sở nhập khẩu thực hiện việc nhập khẩu trang thiết bị y tế phải đồng thời gửi văn bản ủy quyền đó cho cơ quan cấp số lưu hành và cơ quan hải quan;
b) Có kho và phương tiện vận chuyển đáp ứng yêu cầu theo quy định tại khoản 2 Điều 37 Nghị định này hoặc có hợp đồng với cơ sở có đủ năng lực để bảo quản và vận chuyển trang thiết bị y tế;
c) Có kho bảo quản, hệ thống theo dõi quản lý quá trình xuất, nhập, tồn kho trang thiết bị y tế có chứa chất ma túy và tiền chất đáp ứng các yêu cầu theo quy định tại khoản 3 Điều 37 Nghị định này.
3. Trình tự, thủ tục xuất khẩu, nhập khẩu trang thiết bị y tế thực hiện theo quy định của pháp luật về hải quan. Tổ chức nhập khẩu trang thiết bị y tế không phải chứng minh việc đáp ứng các điều kiện theo quy định tại khoản 2 Điều này khi thực hiện thủ tục hải quan.
Điều 47. Điều kiện thực hiện dịch vụ tư vấn về kỹ thuật trang thiết bị y tế
1. Việc thực hiện dịch vụ tư vấn về lập danh mục và xây dựng cấu hình, tính năng kỹ thuật trang thiết bị y tế phải được thực hiện bởi cá nhân đã được cấp giấy chứng nhận đã qua đào tạo về tư vấn kỹ thuật trang thiết bị y tế.
2. Điều kiện của cá nhân thực hiện tư vấn kỹ thuật trang thiết bị y tế:
a) Có trình độ từ đại học chuyên ngành kỹ thuật hoặc chuyên ngành y, dược trở lên;
b) Có thời gian công tác trực tiếp về kỹ thuật trang thiết bị y tế tại cơ sở trang thiết bị y tế từ 05 năm trở lên;
c) Đã được cơ sở đào tạo kiểm tra và công nhận đủ khả năng tư vấn về kỹ thuật trang thiết bị y tế theo chương trình đào tạo do Bộ Y tế ban hành.
3. Người tư vấn chỉ được tư vấn về kỹ thuật trang thiết bị y tế sau khi đã được Bộ Y tế cấp phiếu tiếp nhận hồ sơ công bố đủ điều kiện tư vấn về kỹ thuật trang thiết bị y tế theo quy định tại điểm b khoản 2 Điều 48 Nghị định này.